- Una reacción química es un proceso mediante el cual una o más sustancias (reactivos), se transforman para dar lugar a otras sustancias diferentes(productos). Existen diversas reacciones y de acuerdo a ciertas características; en este blog aprenderemos como poder distinguir solo con ver la ecuación química. Ahora miraremos diferentes clasificaciones.
- CLASES DE REACCIONES QUÍMICAS SEGÚN EL PROCESO QUÍMICO OCURRIDO
- A. REACCIÓN DE SÍNTESIS O COMBINACIÓN: Es donde reaccionan dos o más reactivos(elementos o compuestos) para formar un solo producto(compuesto).
En otras palabras una la sutancia A con la Sustancia B y me forma una sustancia con propiedades químicas diferentes AB.
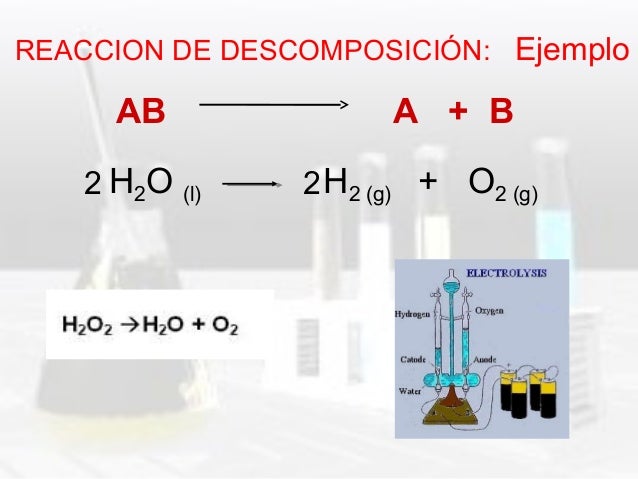
- B. REACCIÓN DE DESCOMPOSICIÓN Un compuesto reacciona, produciéndose dos o mas sustancias simples. El número de moléculas en el producto es mayor que el de los reactivos.
En este caso es completamente contrario a la reacción de síntesis, tenemos una sustancia compleja, es decir siempre encontraremos un compuesto como reactivo y nos formará sustancias más sencillas.
- C. REACCIONES DE DESPLAZAMIENTO
- Se clasifican en
- DESPLAZAMIENTO O SUSTITUCIÓN SIMPLE: Sucede cuando un elemento y un compuesto reaccionan y toma el lugar de un elemento en dicho compuesto desplazando a otro.
Es fácil poder identificar este tipo de reacción pues siempre encuentras en el reactivo un elemento que se encuentra solo, es decir, no esta unido a otro elemento formando un compuesto, como es el caso del "Magnesio", de igual manera encontraremos en el producto un elemento sólito como es el caso del "Cobre". Por lo general siempre sigue ese orden.
- DESPLAZAMIENTO O SUSTITUCIÓN DOBLE: Dos compuestos intercambian átomos o grupo de átomo. Ocurre por lo general los reactivos se encuentran en medio acuoso.
En este tipo de reacciones, solo se presenta entre compuestos químicos, presentes tanto en el reactivo como en el producto. Son ejemplo de este tipo de reacciones la formación de sales mediante la unión de hidróxidos y ácidos.
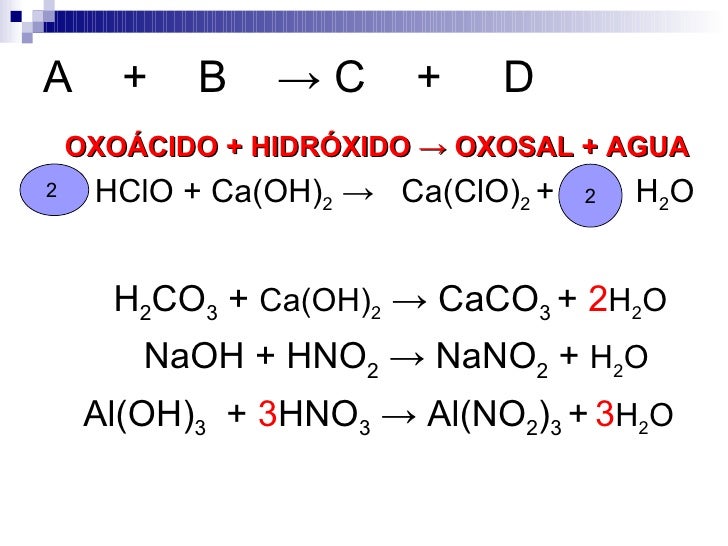
- D. REACCIÓN DE NEUTRALIZACIÓN Son reacciones entre ácidos y bases o también llamado hidróxidos en las que se produce una sal y agua.
- E. REACCIÓN DE PRECIPITACIÓN Son aquellas en las que las sustancias reaccionantes dan lugar a una fase sólida insoluble o precipitado.
Para identificar la reacción de precipitación es sencillo, pues encontraras una flecha hacia abajo en uno de los compuestos del producto
- F. REACCIÓN DE OXIDACIÓN-REDUCCIÓN: Se caracteriza por que los electrones se transfieren de una sustancia a otra. Si una sustancia pierde electrones se oxida y si gana electrones se reduce.
En esta clase de reacción es necesario manejar los estados de oxidación de los elementos en el compuesto, para saber cual cambio de estado de oxidación y de esa forma sabrás que pertenece a este tipo de reacción. miremos el ejemplo:
Si vemos el ejemplo podemos notar que el Zinc en el reactivo su estado de oxidación era cero y en el producto paso a ser +2 (según la tabla arriba el Zn se oxidó) , en cambio en el Hierro paso al contrario de tener en el reactivo un estado de oxidación +2, paso en el producto a 0 ( según la tabla arriba se redujo)
- G. REACCIÓN DE COMBUSTIÓN Consiste en una combinación química de una sustancia con el oxígeno de la atmósfera para dar dióxido de carbono o monóxido de carbono y agua.
Esta reacción es sencilla de identificar pues en el reactivo siempre estará presente el oxígeno atmosférico con un hidrocarburo (compuesto de carbono e hidrógeno) y en el producto tendremos CO o CO2 con agua.
- CLASIFICACIÓN DE LAS REACCIONES QUÍMICAS SEGÚN EL SENTIDO EN EL QUE SE LLEVE A CABO LA REACCIÓN
- REACCIONES REVERSIBLES Se realizan simultáneamente en los 2 sentidos, creándose una situación de equilibrio químico en el cual el flujo de sustancias en ambos sentidos es similar.
- REACCIÓN IRREVERSIBLE Los reactivos reaccionan para convertirse en los productor sin la posibilidad de que estos originen nuevamente los reactivos. El sentido de la flecha es único.
Esta es la clasificación más sencilla, pues la flecha que hay en medio de los reactivos y el producto, determina si es una reacción reversible o irreversible.
- CLASIFICACIÓN DE LAS REACCIONES QUÍMICAS TENIENDO EN CUENTA LOS CAMBIOS ENERGÉTICOS PRODUCIDOS
- REACCIONES EXOTÉRMICAS Es una reacción química que produce o libera energía, la cual se presenta casi siempre como calor, también se puede expresar como KJ (Kilojulios)
- REACCIONES ENDOTÉRMICAS Es una reacción química que absorbe energía para que ocurran las transformaciones químicas, es decir, la energía es suministrada del entorno para que se efectúe la reacción en la mayoría de casos en forma de calor.
En este caso la reacción endotérmica presenta el calor en el reactivo.





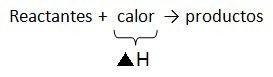

muy interesante felicidades
ResponderEliminar